
|

|
2012年11月20日,FDA批准艾曲波帕(商品名:Promacta)用于治疗慢性丙型肝炎患者的血小板减少症,以便使这些患者能够启动并维持以干扰素为基础的肝病标准疗法。它是获批用于此类患者的首个支持性护理药物。
艾曲波帕最初于2008年11月获得FDA批准在美国上市,被批准用于一种称为慢性免疫性血小板减少性紫癜的罕见疾病的治疗。
2010年9月23日卫生部印发《过敏性紫癜等6种疾病诊疗指南》,《指南》对特发性血小板减少性紫癜的主要临床表现描述为皮肤、黏膜广泛出血,多形成散在性的皮内或皮下出血点,继而形成瘀点及瘀斑。另外,球结膜下出血也是常见症状。
特发性血小板减少性紫癜(ITP)是一种免疫介导的血小板减少综合征, 是临床最为常见的出血性疾病, 约占出血性疾病总数的30%, 欧美国家年发病率为5~10/10万人口,可发生在任何年龄阶段。我国尚无ITP发病的流行病学资料。一般认为该病的发生是由于自身抗体致敏的血小板被单核巨噬细胞系统过渡破坏。
防止血小板被破坏是治疗ITP患者的主要方法。鉴于ITP的良胜疾病性质, 致死性出血的风险与致死性治疗相关并发症的发生率大致相当, 对ITP患者应尽量避免过度治疗。目前的治疗方案有长期服用泼尼松或大剂量地塞米松冲击治疗;脾切除疗法;幽门螺杆菌根除疗法;重组人血小板生成素治疗及利妥昔单抗疗法等。但上述各方法有的有严重的不良反应,有的手术易出现感染等并发症等等,临床需要更好治疗方案,于是艾曲波帕和罗米司亭应运而生。
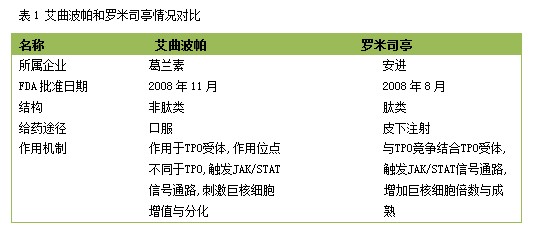
临床应用过程中,患者对艾曲波帕和罗米司亭表现出良好的耐受性, 常见的不良反应为头痛、疲劳、关节痛等。可持续给药维持疗效。鉴于良好的临床表现,上市以来,艾曲波帕和罗米司亭为两大制药巨头带来的可观的利润。
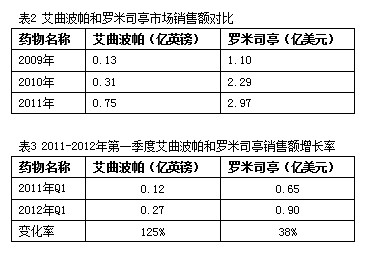
中国是全球最大最有活力的新兴市场,特别是在欧元区经济持续低迷,美国市场持续疲软,市场需求不断下降的情况下,国外制药企业表达了对中国市场的极大重视,艾曲波帕和罗米司亭进入中国的脚步越来越近。据米内网-药品审评数据库显示,葛兰素公司的艾曲波帕于2012年9月获得SFDA批准临床,而安进公司的罗米司亭于2012年11月向SFDA提出申报临床。(来源:米内网)
